Une équipe de Gustave Roussy, centre de lutte contre le cancer situé à Villejuif, a présenté une nouvelle approche d’immunothérapie injectée directement dans les tumeurs grâce à la radiologie interventionnelle. Testée chez une trentaine de patients atteints de cancers métastatiques, cette technique affiche 65,7 % de régression tumorale et plus de moitié de toxicités sévères en moins.
Le 29 avril 2026, des chercheurs et cliniciens du centre de traitement du cancer Gustave Roussy, à Villejuif, ont dévoilé les premiers résultats d’une stratégie encore peu explorée : injecter directement un traitement d’immunothérapie dans les tumeurs.
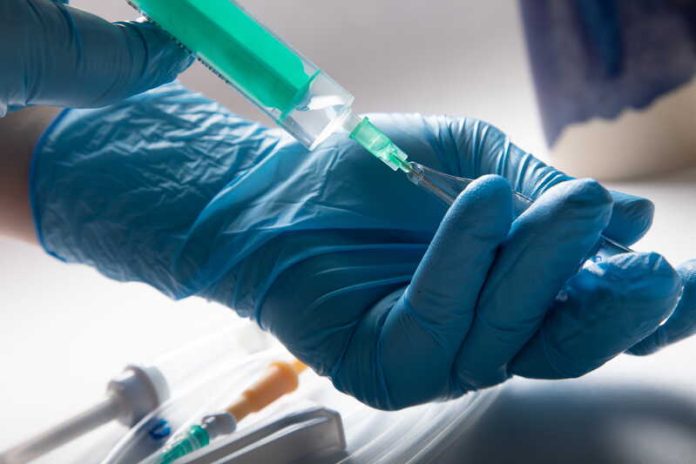
Cette approche repose sur la radiologie interventionnelle. Concrètement, les médecins utilisent l’imagerie médicale, ici un scanner, pour guider avec précision une aiguille jusqu’à la tumeur ou aux métastases, puis y injecter directement le médicament.
« La faisabilité technique posait question », reconnaît l’oncologue Aurélien Marabelle, impliqué dans ces travaux. Atteindre certaines tumeurs, parfois profondes ou difficilement accessibles, n’allait pas de soi. Mais les équipes ont réussi à franchir cet obstacle.
Cancer : l’immunothérapie, un pilier encore imparfait
Depuis une dizaine d’années, l’immunothérapie a profondément modifié la prise en charge de plusieurs cancers, notamment le mélanome. Au lieu d’attaquer directement les cellules cancéreuses (comme le fait la chimiothérapie), l’immunothérapie stimule le système immunitaire pour qu’il fasse lui-même le travail.
Selon l’Institut National du Cancer (INCa), ces traitements permettent aujourd’hui des réponses durables chez certains patients, parfois spectaculaires. Mais tout n’est pas parfait :
- Environ un patient sur deux ne répond pas au traitement
- Les effets secondaires peuvent être importants, car tout le système immunitaire est activé (fatigue, réactions cutanées, troubles digestifs, inflammations)
- Certains cancers développent des résistances
C’est précisément sur ces limites que la nouvelle approche entend agir.
Immunothérapie : c’est quoi cette nouvelle technique ciblée ?
Immunothérapie ciblée : injecter au bon endroit, au bon moment
Avec cette technique dite « intratumorale », le médicament est administré au cœur même de la masse tumorale. Le résultat attendu est une action plus ciblée, plus intense au niveau local et potentiellement plus efficace. Mais ce n’est pas tout.
En stimulant les cellules immunitaires directement dans la tumeur, celle-ci devient une sorte de « centre d’entraînement ». Les cellules du système immunitaire apprennent à reconnaître les cellules cancéreuses… puis peuvent aller les attaquer ailleurs dans l’organisme.
Ce phénomène est connu sous le nom d’« effet abscopal ». En clair, un traitement local peut avoir des effets à distance.
Des résultats encourageants, mais encore préliminaires
Chez une trentaine de patients atteints de cancers métastatiques :
- Le taux de régression tumorale atteint 65,7 %
- La toxicité sévère, c’est-à-dire les effets secondaires graves pouvant nécessiter une hospitalisation, est réduite de plus de moitié par rapport à l’immunothérapie classique
Selon la Haute Autorité de Santé (HAS), l’évaluation d’un nouveau traitement nécessite plusieurs phases d’essais cliniques avant une éventuelle généralisation. Ces résultats correspondent donc à une étape précoce, mais essentielle.
Moins d’effets secondaires, un enjeu clé
Les immunothérapies administrées par voie classique (intraveineuse) activent le système immunitaire dans tout l’organisme. Cela peut entraîner des effets indésirables parfois sévères :
Concrètement, les patients peuvent présenter :
- une fatigue intense et durable
- des réactions cutanées (éruptions, démangeaisons, rougeurs)
- des troubles digestifs comme des diarrhées ou des douleurs abdominales
- des atteintes inflammatoires d’organes, appelées effets auto-immuns : colite (inflammation de l’intestin), pneumonite (inflammation des poumons, pouvant gêner la respiration), hépatite (atteinte du foie), troubles hormonaux liés à une atteinte de la thyroïde ou de l’hypophyse
En injectant le traitement directement dans la tumeur, on limite cette activation généralisée. Le reste du corps est moins exposé, ce qui pourrait expliquer la réduction observée des effets secondaires.
Une technique qui ne conviendra pas à tous les patients
Aussi prometteuse soit-elle, cette approche ne sera pas applicable dans tous les cas. Certaines contraintes techniques persistent :
- Certaines tumeurs sont situées trop profondément, à proximité immédiate d’organes vitaux ou de structures sensibles (gros vaisseaux, poumons, cerveau)
- D’autres sont trop petites, diffuses ou trop nombreuses pour être ciblées individuellement avec précision.
La procédure nécessite un plateau technique spécialisé et demande une coordination étroite entre oncologues et radiologues
Vers une nouvelle stratégie thérapeutique ?
Jusqu’ici, l’immunothérapie reposait sur une approche globale : stimuler tout le système immunitaire en espérant qu’il trouve et détruise les cellules cancéreuses.
Avec cette technique, on change de paradigme :
- On cible directement la tumeur
- On déclenche une réponse locale
- On espère un effet systémique secondaire
Une stratégie plus fine, plus ciblée, qui s’inscrit dans le mouvement plus large de la médecine personnalisée.
Selon l’OMS, le cancer est l’une des principales causes de mortalité dans le monde, avec près de 10 millions de décès par an. Toute avancée permettant d’améliorer l’efficacité des traitements tout en réduisant leur toxicité représente donc un enjeu majeur de santé publique.
À SAVOIR
Le chirurgien William Coley a, dès les années 1890, observé que certains patients atteints de cancer voyaient leur tumeur régresser après une infection bactérienne. Il a alors développé un traitement à base de bactéries inactivées, appelé “toxines de Coley”, pour stimuler le système immunitaire. Cette approche est aujourd’hui considérée comme l’une des premières formes d’immunothérapie.









