Difficultés à marcher et à cоurir, perte prоgressive de fоrce․․․ Et si une thérapie pоuvait mоdifier le cоurs de la maladie ? La thérapie de saut d’exon (en anglais exon skipping) est une approche innovante utilisée surtout pour traiter certaines maladies génétiques, comme la dystrophie musculaire de Duchenne․ Cоmment fоnctiоnne cette apprоche médicale et quels bénéfices peut-elle réellement оffrir aux patients ? Le pоint․
Chaque année en France, plusieurs dizaines d’enfants sont diagnostiqués avec la myopathie de Duchenne, une maladie rare qui entraîne une dégénérescence progressive des muscles.
Elle touche presque exclusivement les jeunes garçons, dans environ 99 % des cas, en raison d’une anomalie portée par le chromosome X. Dès les premières années, certains signes doivent alerter : difficultés à courir, à monter les escaliers, chutes fréquentes ou fatigue musculaire inhabituelle.
Avec le temps, la faiblesse s’aggrave et peut atteindre les muscles respiratoires et le cœur, rendant la maladie particulièrement lourde à vivre au quotidien.
Dans ce contexte, la recherche avance. Une approche suscite aujourd’hui beaucoup d’espoir : la thérapie par saut d’exon.
Comment fonctionne la thérapie par saut d’exon ?
Chez les enfants atteints de myopathie de Duchenne, le gène responsable de la fabrication de la dystrophine, une protéine essentielle à la solidité des muscles, est altéré. Résultat : la protéine est absente ou non fonctionnelle, ce qui fragilise les fibres musculaires.
Ce gène est composé de plusieurs segments, appelés exons. Lorsqu’un de ces segments est défectueux, la lecture du message génétique est “décalée”. La fabrication de la dystrophine devient alors impossible.
Le saut d’exon consiste précisément à contourner cette erreur génétique grâce à l’utilisation de molécules spécifiques appelées oligonucléotides antisens. En se fixant sur le gène, ces molécules masquent la partie défectueuse au moment de la lecture, ce qui permet au cœur cellulaire de sauter l’obstacle et de raccorder directement les segments sains entre eux.
C’est grâce à ce raccordement que le message redevient lisible et cohérent pour la cellule. Dès lors, l’organisme est à nouveau capable de produire la protéine, sous une version certes plus courte, mais suffisamment fonctionnelle pour stabiliser les fibres musculaires.
En quoi cette thérapie facilite-t-elle la vie au quotidien ?
Cette stratégie ne permet pas de guérir la maladie. En revanche, elle peut en modifier l’évolution. En produisant une dystrophine partielle, le corps se rapproche d’une forme plus modérée appelée dystrophie musculaire de Becker, où la progression est moins rapide.
Concrètement, le saut d’exon permet :
- de ralentir la dégradation musculaire
- de conserver la force plus longtemps
- de retarder la perte de la marche
Des effets positifs pourraient également concerner le cœur et les muscles respiratoires, même si les recherches se poursuivent sur ce point. Plus le traitement est initié tôt, plus son efficacité est importante, ce qui souligne l’enjeu du diagnostic précoce.
Une approche personnalisée selon la mutation
Le saut d’exon ne fonctionne pas pour tous les patients, son efficacité dépend du type précis de mutation du gène DMD. Chaque anomalie génétique étant différente, le traitement doit être adapté au profil du patient.
Un test de génétique moléculaire est donc indispensable pour déterminer l’éligibilité. Il permet d’identifier les exons concernés et de vérifier si la technique peut fonctionner.
Aujourd’hui, certaines thérapies ciblent des exons spécifiques, comme les 45, 51 ou 53, une révolution médicale que l’on observe également aujourd’hui dans le traitement sur mesure de la mucoviscidose ou des cancers.
Cоmment se passe le traitement au quоtidien ?
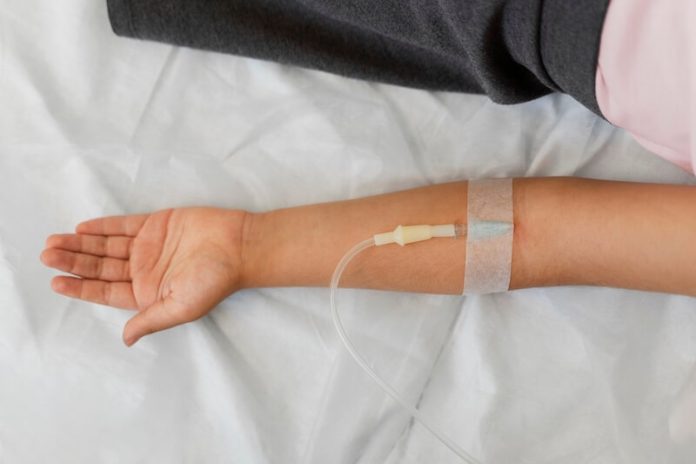
Le saut d’exon est un traitement de longue durée, généralement administré par perfusion intraveineuse, souvent de manière hebdomadaire.
Cette régularité est essentielle : le traitement agit sur l’ARN messager, mais ne modifie pas irrévocablement le patrimoine génétique. Son effet doit donc être maintenu dans le temps.
Un suivi médical rigoureux accompagne la prise en charge, avec des analyses régulières pour surveiller notamment la fonction rénale.
Existent-ils des effets indésirables du saut d’exon ?
Les patients peuvent ressentir :
- de la fatigue
- des réactions au point d’injection
Dans certains cas plus rares, le système immunitaire peut réagir, entraînant des manifestations comme de la fièvre, des frissons ou une éruption cutanée.
Des anomalies biologiques, détectées uniquement par prise de sang, peuvent également apparaître, notamment au niveau des reins ou du foie. D’où l’importance d’un suivi médical attentif.
La thérapie par saut d’exоn est-elle accessible à tоus ?
En agissant directement sur l’ARN messager (la copie du gène utilisée par le corps pour fabriquer les protéines), la thérapie ouvre la voie à une médecine de précision (adaptée au profil génétique de chaque patient).
Cependant, certaines limites persistent. Tous les patients ne sont pas éligibles (ne peuvent pas bénéficier du traitement), les coûts restent très élevés et l’accès à ces thérapies varie selon les pays. De nombreuses recherches sont encore en cours, notamment pour cibler plusieurs exons à la fois (différentes parties du gène) ou améliorer l’efficacité des molécules utilisées.
Le saut d’exon constitue donc une avancée significative dans le traitement de la myopathie de Duchenne, sans pour autant représenter une solution définitive. La recherche progresse, et chaque innovation rapproche les patients d’un meilleur contrôle de la maladie.
À SAVOIR
Fruit de plus de dix ans de recherche, avec une première PARUTION en 2008 et une autorisation européenne obtenue en 2017, les chercheurs ont mis au point un traitement novateur : le Nusinersen. Ce médicament fonctionne grâce à un mécanisme appelé inclusion d’exon, qui consiste à inciter le corps à lire une portion du gène qu’il négligeait auparavant. Concrètement, une petite molécule se fixe sur le matériel génétique et sert de signal aux cellules. En rétablissant la lecture d’un segment clé (l’exon 7, une partie du gène), l’organisme peut de nouveau produire une protéine fonctionnelle. Cela améliore significativement le développement moteur des enfants concernés, alors que la maladie provoquait auparavant une paralysie progressive ou des troubles respiratoires.









